ANViSa,全称Agência Nacional de Vigilancia Sanitária,隶属巴西卫生部,负责所有医疗器械、体外诊断产品及其他健康相关产品(如药品、卫生用品、化妆品等)的上市前与上市后的管控。
INMETRO,全称INSTITUTO NACIONAL DEMETROLOGIA,NORMALIZAÇÃO E QUALIDADE INDUSTRIAL,隶属巴西发展、工业及外贸部,负责对产品认证及计量管理。INMETRO制定了116种(至2015年5月)产品的强制认证要求。包括七大健康产品和四种医疗器械,7大类健康产品的INMETRO证书及4种医疗器械的强制计量证书是进行ANViSa注册的必须文件之一。
ANViSa将医疗器械按照其风险的高低分为4个等级,从低到高分别为Class I, Class II, Class III和Class IV。其中III和IV类产品在产品上市前需通过巴西BGMP RD16质量体系审查(或MDSAP认证)。其中I,II类注册证永久有效,III和IV类注册证有效期为10年。
流程图:
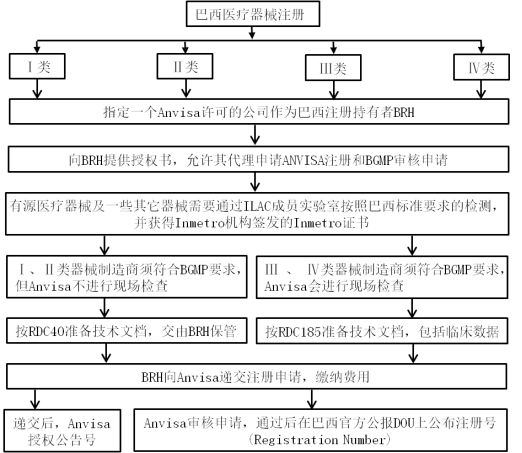
通用法规:
RDC No.16,2013- Technical regulation of good manufacturing practices for
Medical devices and products for in vitro diagnostic useRDC NO. 185,2001-registration of medical products at ANVISA
RDC NO. 40,2015- Defines all medical product cadastro registration requirements
In vitro Device RDC 36/2015
Ordinance No.384/2020
官方时间和费用:
官方时间
ANVISA审批时间:6个月;
官方费用
注册费用以官网上公示的费用为准;
相关业务:
ANVISA技术文件代理
INMETRO认证辅导
BGMP验厂辅导
MDSAP质量体系辅导
BRH巴代服务