加拿大卫生部(Health Canada)负责在医疗器械在加拿大上市销售之前对其进行审查,以评估其安全性和有效性。加拿大将医疗器械按产品风险程度分为四个(I, II, III, IV)风险等级。所有风险等级的医疗器械在加拿大销售,都必须获得医疗器械营业许可证Medical Device Establishment Licence(MDEL)。其中 I类豁免MDL申请,I类只需要申请MDEL,而II类, III类和IV类医疗器械申请医疗器械注册证Medical Device Licence(MDL)。
参加对象:
管理者代表
总工程师
研发经理
质量经理
产品注册专员
标准和法规工程师
风险管理工程师
项目经理
研发工程师
工艺工程师
质量工程师
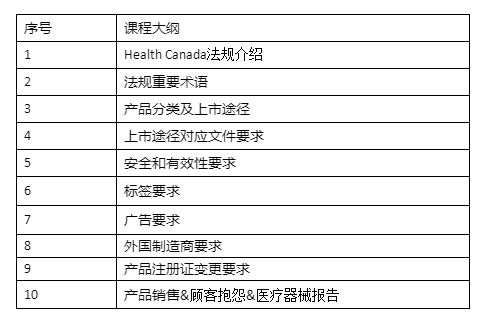
课程大纲: