2013年9月美国食品药品管理局(Food and Drug Administration, FDA)发布医疗器械唯一标识系统(unique device identification system, UDI system)法规正式启动UDI实施工作
(1)UDI定义
UDI(Unique Device Identifier)基于标准创建的一系列由数字、字母数字符号组成的代码,包括产品标识和生产标识,用于对医疗器械进行唯一性识别。
(2)UDI构成
UDI=DI+PI
● DI=Device Identifier
产品标识
是特定于某种规格型号医疗器械的唯一性代码,可用作对医疗器械唯一标识数据库存储信息的“访问关键字”。
● PI=Production Identifier
生产标识
识别医疗器械生产过程相关数据的代码,根据实际应用需求可包含医疗器械序列号、生产批号、生产日期、失效日期等。
(3)发码机构
GS1:Globe standard 1
HIBCC:Health Industry Business Communicatios Council
ICCBBA:International Council for Commonality in Blood Banking Automation
流程图
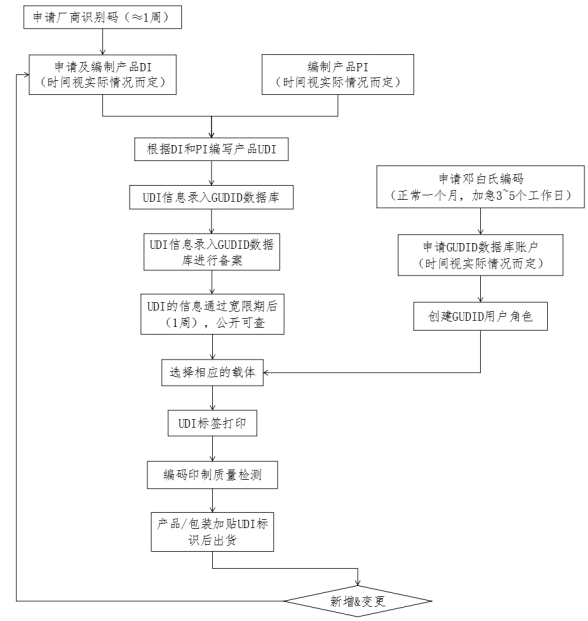
通用法规
21 CFR part 830 唯一医疗器械标识;
21 CFR part 801 标识;
21 CFR part 803 医疗器械报告;
21 CFR part 806 医疗器械,纠正与移除的报告;
21 CFR part 810 医疗器械召回;
21 CFR part 814 入市前许可;
21 CFR part 820 质量体系法规;
21 CFR part 821 医疗器械追踪的要求;
21 CFR part 822 上市后的监管。
官方时间和费用
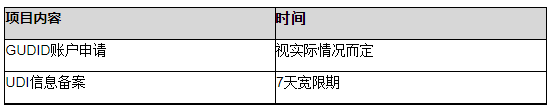
实施时间

官方费用
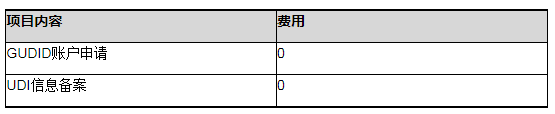
官方时间